生物醫用材料作為一類先進多功能材料可用于診斷、治療、修復或替代人體組織、器官或增進其功能,其獨特療效為藥物不可替代。從醫用鈦合金材料的研發歷史和長期臨床應用反饋表明,其未來發展重點依然是先通過研究其體外的生物相容性、力學相容性等基礎科學問題,最終才能實現解決或改善其體內的生物安全性和服役長效性問題。提高醫用鈦合金材料的生物及力學相容性是確保其在體內長期穩定服役并發揮持久治療效果的關鍵,也是設計和開發新型醫用鈦合金材料的研究基礎和應用目標。本文從醫用鈦合金材料合金設計、物理冶金、材料加工、組織與性能、表面改性、先進制造及臨床應用等諸方面進行了綜述,并介紹了作者研發團隊的最新進展,展望了未來發展趨勢及待解決的問題。
合金化設計及新型合金材料開發
目前市場上外科植入物和矯形器械常用的金屬原材料主要包括不銹鋼、Co-Cr基合金和鈦合金3大類,約占整個生物材料產品市場份額的40%左右 。
鈦合金具有密度小、比強度高、生物及力學相容性較好及易加工成型等特點,已發展成為一類量大面廣的中高端外科植入物用的主要原材料。從鈦合金牙種植體、人工關節等骨科硬組織修復替代到冠脈支架等血管及軟組織微創介入等高端金屬器械產品的里程碑式的應用至今,對其遠期療效暴露出的各種失效問題促使人們不斷優化和改良傳統的醫用鈦合金材料,同時積極研究和開發新型優良的醫用鈦合金材料。

1、醫用鈦合金材料的研發概述
鈦合金在生物醫學領域的研究可追溯到上世紀40年代初期,Bothe等和Leventhal通過動物實驗最先證實了純Ti的良好生物安全性;上世紀50~60年代,不銹鋼和Co-Cr合金得到廣泛應用,而具有中低強度的α型鈦合金包括純Ti和Ti3A12.5V鈦合金(TA18)開始在口腔種植體等承載較小的骨齒科部位獲得開發和應用嘗試 。上世紀70年代后期,航空用具有中高強度的兩相鈦合金Ti6A14V ( α +β 型,TC4、TC4ELI)開始移植到醫學領域并迅速獲得推廣應用。隨著鈦合金在臨床應用的不斷深入,臨床醫生在實施TC4鈦合金人工髖關節翻修手術時發現其生物學和生物力學性能不盡人意。上世紀90年代中期,瑞士和德國先后開發出以Nb和Fe分別替代V的新型醫用兩相鈦合金Ti6Al7Nb (TC20)和
Ti5Al2.5Fe (TC15) ;但是隨后發現上述2種合金在生物安全性、生物力學相容性和加工成型性等方面仍有缺陷(Ti5Al2.5Fe合金已被國際醫學標準廢棄),且它們較高的彈性模量與TC4鈦合金相當,這不利于與具有較低彈性模量的骨組織的生物力學性能相匹配。
上世紀90年代人們開始研發不含有毒元素、高強度、低模量的第三代新型β 型(包括全β型、亞穩β型、近β型或稱富α +β 型)醫用鈦合金,已開發成功的新型β 型鈦合金主要包括美國開發的Ti13Nb13Zr、日本開發的 Ti15Mo5Zr3Al、德國開發的 Ti30Ta 等合金。我國從上世紀80年代開始醫用鈦合金材料的研究與開發,1999年西北有色金屬研究院在國內首次研制出第一個具有我國自主知識產權的近α 型醫用鈦合金Ti3Al2Mo2Zr (TA24),2002 年研制出2種新型近 β型醫用鈦合金 Ti-5Zr-5Mo-15Nb(TLE)和Ti-5Zr-3Sn-5Mo-15Nb(TLM) 。另外,中國科學院金屬研究所、東北大學、哈爾濱工業大學、北京有色金屬研究總院、寶雞有色金屬加工廠等單位也開展了新型 β型鈦合金的基礎和應用研究。我國在醫用β型鈦合金研發方面已走在國際前列,但尚無β型鈦合金納入我國外科植入物材料國家標準。
2、醫用鈦合金化設計及開發
2.1 醫用鈦合金化選材設計 開展新型醫
用鈦合金化選材設計時,合金添加元素的細胞毒性是首要考慮因素,同時要求所添加元素對鈦合金綜合力學性能的不良影響最小。金屬Ti具有同素異構相轉變,在882 ℃時從低溫的α相(hcp結構)轉變為高溫的 β 相(bcc結構)。根據合金元素在α 相和β相中的溶解度(或根據它們對相變溫度的影響),可將其合金元素大致分為α 相穩定元素、β相穩定元素和中性元素。目前國內外學者在進行醫用鈦合金化選材設計時,主要選用對人體有益的鈦合金β相穩定元素Nb、Mo、Ta、Hf和中性元素Zr、Sn以及α 相穩定元素Al、O、N等合金元素,而選材基本原則是根據合金元素在Ti及鈦合金中的作用及相圖決定的:一是利于新合金形成單一均勻相(替代式或間隙式固溶體),避免形成金屬間化合物等硬質脆性相組織;二是通過影響α +β/ β相變點,有利于后續的加工、熱處理和顯微組織及力學性能調控。
目前國內外已報道的各類新型醫用鈦合金多達近百個,合金設計包括二元系到六元系合金,合金元素涉及近20個 。一般來講,α 相穩定元素Al、O、N等對鈦合金的強化非常有效,但通常降低材料的塑韌性并提高其彈性模量;而Zr、Nb、Mo、Sn能夠使Ti基體強化而對塑韌性的不利影響較小,同時對降低彈性模量有利。Song等通過對β型二元鈦合金中添加元素的電子結構計算也同樣證實中性元素Zr和β相穩定元素Mo、Ta、Nb有利于降低合金的彈性模量,而α 相穩定元素Al可增加彈性模量,改變中性元素Sn在TiNbSn合金中的含量對合金低屈服應力和超彈性也有一定影響。針對新型β鈦合金成分多元化和力學相容性設計要求,除了需嚴格選擇和控制合金元素特別是β相穩定元素及配比(重量或原子比),特別需要關注合金多元化后對性能的耦合影響,因為已經證實Zr、Sn、Mo、Nb、Ta等元素對多元鈦合金強度、塑性和模量等理化性能的影響,與其在合金中配比存在非線性或定量依存關系,不同元素對合金性能的影響各不相同,力學性能隨著合金成分的變化顯得更加復雜,這與二元合金的影響規律不盡相同 。O和N等氣體雜質元素在提高合金強度的同時也使得彈性模量增大,因此通常按照微量元素來加入以調整其塑韌性及彈性允許應變 。另外,Hf、Ta、Nb元素雖然對合金低模量化和加工塑韌性調控有利,但原材料價格昂貴、熔點較高,不適于低成本化鈦合金設計選材。

2.2 醫用鈦合金化設計方法概述
對于新型高強度低模量的介穩定β鈦合金的設計開發,當前國際上大多采用Mo當量公式、K b 穩定化系數、d-電子合金理論、平均電子濃度e/a、第一性原理和分子軌道理論等方法進行合金成分設計和組織性能的預測。此外,借助合金元素的熱力學和動力學參數、不同相晶格參數等建立數據庫或實驗模型,結合計算分析軟件和方法也開發了諸如[團簇](連接原子) x 結構模型、神經網絡技術、模糊邏輯等方法,這些合金設計方法經實驗驗證均取得了較理想的效果 。
Mo當量設計方法是目前獲得高強度鈦合金最簡便有效的途徑之一。它主要通過事先計算出各種合金添加元素的“Mo當量”數值來預測合金的相結構與力學性能:當Mo當量在0~9之間時,隨Mo當量的增加,強度相應提高。而d-電子合金設計法是基于不同類型鈦合金在電子軌道相圖上的位置區間,以及彈性模量和強度在相圖上的排列規律來進行醫
用鈦合金的設計:其一般設計準則是首先確定合金具有低模量的電子軌道參數,然后根據不同合金元素的電子軌道參數及d-電子理論,計算出合金的平均電子軌道參數,使之符合設定的目標。目前許多新型醫用低模量 b 鈦合金采用該方法進行合金設計。此外,根據平均價電子數與彈性模量的相關曲線規律,當平均價電子數為4.2~4.25時合金模量
較低,日本學者采用此法率先開發出了基本成分為Ti(Nb、Ta、V)+(Zr、Hf)+O的低模量 b 鈦合金-橡膠金屬,該合金的平均價電子數約為4.24,其彈性模量與人體骨接近,但強度等性能較低而未在外科植入物領域獲得實際應用 。Hu等 發明的新型Ti2448(Ti24Nb4Zr7.6Sn)鈦合金,其平均價電子數只有4.15,理論上并不在低模量區間,但實際模量最低可達40 GPa。因此,該法對新型醫用鈦合金的設計不具普適性。模糊邏輯和神經網絡技術的合金設計法首先都需要大量的合金成分及相應的性能數據,然后使用模糊邏輯推理軟件或神經網絡軟件建立合金成分與性能的數學模型,再利用其它數據進行不斷修正以達到對合金成分優化和性能預測的目的,但該類設計方法目前尚不完善 。
1.2.3 新型醫用鈦合金的開發 目 前 國 際 上
已設計成功的低模量醫用β鈦 合 金 多 達 20余 種 ,已 被 納 入 國 際 標 準 的 新 型 醫 用 β鈦 合金 有 Ti13Nb13Zr、Ti12Mo6Zr2Fe (TMZF)、Ti15Mo、Ti15Mo5Zr3Al和Ti45Nb等,其中前3種是為了降低應力屏蔽效應和提高其生物力學相容性的要求由美國設計開發的 。Ti15Mo5Zr3Al 是日本神戶制鋼在 Ti15Mo 的基礎上按照提高耐蝕性和強度
的要求進行設計的。Ti45Nb合金起初也是由美國按航空航天用緊固件等零部件的要求進行設計,隨后由于其高強度、低模量和耐蝕性好等綜合性能而被引入生物醫學工程領域 。隨著低模量β鈦合金的不斷應用,日本開展了大量的研究開發工作,其中日本大同特殊鋼公司基于DV-X a 理論采用d-電子合金設計方法開發出了彈性模量最低約55GPa 的 Ti29Nb13Ta4.6Zr (TNTZ)亞穩β鈦合金。為了降低TNTZ合金成本和彈性模量,提高其強度及疲勞性能,Niinomi 等又分別通過添加不同含量的 O 元素和 Cr 元素以及采用大塑性變形、累積連續冷軋、變形誘發相變、熱機械處理等方法來優化合金的強度、彈性模量、塑性和超彈性等綜合力學性能,揭示了 TNTZ 合金的模量隨高壓扭轉次數或織構的增加而降低以及單晶 TNTZ對晶體取向的依賴性;通過提高O 含量來抑制無熱 w 相的生成,增加Cr元素和合金冷變形使其彈性模量從64 GPa提高至77 GPa,并因此提出了脊柱固定器用“自調節模量”類鈦合金的設計方法。
目前,能夠達到模量自調節的新型鈦合金除了Ti-Cr 系合金,隨后又開發了 Ti17Mo、Ti30Zr5Cr、Ti30Zr7Mo、Ti30Zr3Mo3Cr等合金。日本科研人員設計的低模量鈦合金大多是在TNTZ基礎上陸續發展的,主要通過改變合金元素及其成分并立足低成本化理念來進行設計和研究 ,其應用方向不僅僅限于生物醫學工程領域。
西北有色金屬研究院自上世紀80年代開始致力于各類醫用鈦合金材料的設計和開發,尤其是在鈦合金材料的產業化應用研究方面走在國際前列。
自 1999 年以來已先后開發出 Ti2.5Al2.5Mo2.5Zr(TAMZ)、Ti3Zr2Sn3Mo25Nb (TLM)、Ti15Nb5Zr3Mo(TLE)、Ti10Mo6Zr4Sn3Nb (TB12)等多種新型醫用鈦合金并均獲國家發明專利。2002年于振濤教授研發團隊研制出了2 種新型介穩定β型鈦合金TLM、TLE,其設計原則是:(1) 選擇對人體無毒性、可在α -Ti和 β -Ti中充分固溶以及較低成本的合金元素,并選定Ti-Nb二元系作為合金設計的基礎體系;
(2) 采用d電子理論、Mo當量經驗公式及K b 穩定系數相結合的方法,根據鈦合金二元相圖及d電子軌道相圖計算,選擇能夠產生亞穩態相變及馬氏體轉變而使合金室溫下處于介穩定相狀態的設計參數;
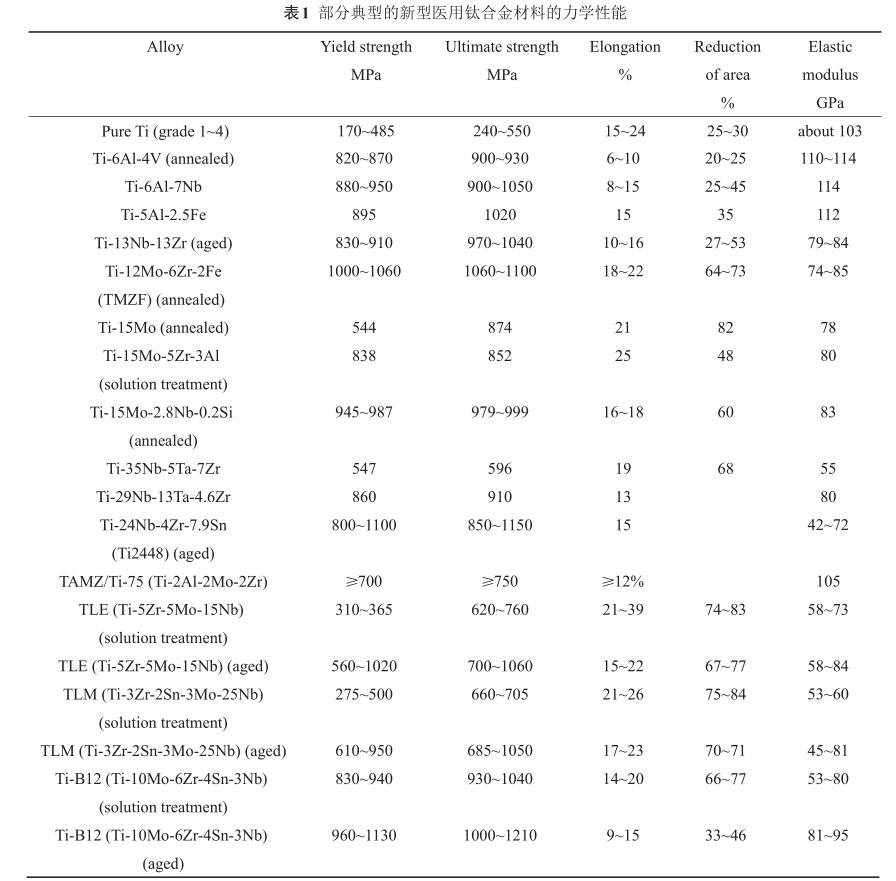
(3) 依據第一性原理計算了合金元素Sn、Zr、Mo及其含量對鈦合金強度、模量及馬氏體轉變溫度等因素的影響,并預先充分考慮了鈦合金冷、熱加工成型性特點,最后通過一系列工業實驗驗證而成功獲得了具有綜合力學性能寬泛且可調控的新型高強度低模量醫用鈦合金,該研發團隊開發的系列新型醫用鈦合金的典型力學性能如表1所示。
相關鏈接










